Lehrgang Qualitätsmanager Medizintechnik nach ISO 13485
Die Weiterbildung vermittelt Dir das Wissen und die Fähigkeiten zum Aufbau integrierter Managementsysteme nach ISO 13485:2016 und zu den regulatorischen Anforderungen – inklusive MDR/IVDR – über den vollständigen Lebenszyklus eines Medizinprodukts.
Zielgruppe:
Der Lehrgang orientiert sich an den neusten Anforderungen (ISO 13485:2016, MDR, IVDR).
Du bist…
- als Fachperson im Qualitätsmanagement und in der Qualitätssicherung für die Erfüllung spezifischer Anforderungen bei der Entwicklung, Zulassung, Herstellung und Überwachung von Medizinprodukten verantwortlich und möchtest Dein Wissen in diesem Themenumfeld schnell und kompakt auf den neusten Stand bringen.
- eine Qualitätsmanagement-Fachperson, die aus einer anderen Branche in den Bereich Medizinprodukte wechseln möchte.
Inhalte detailliert
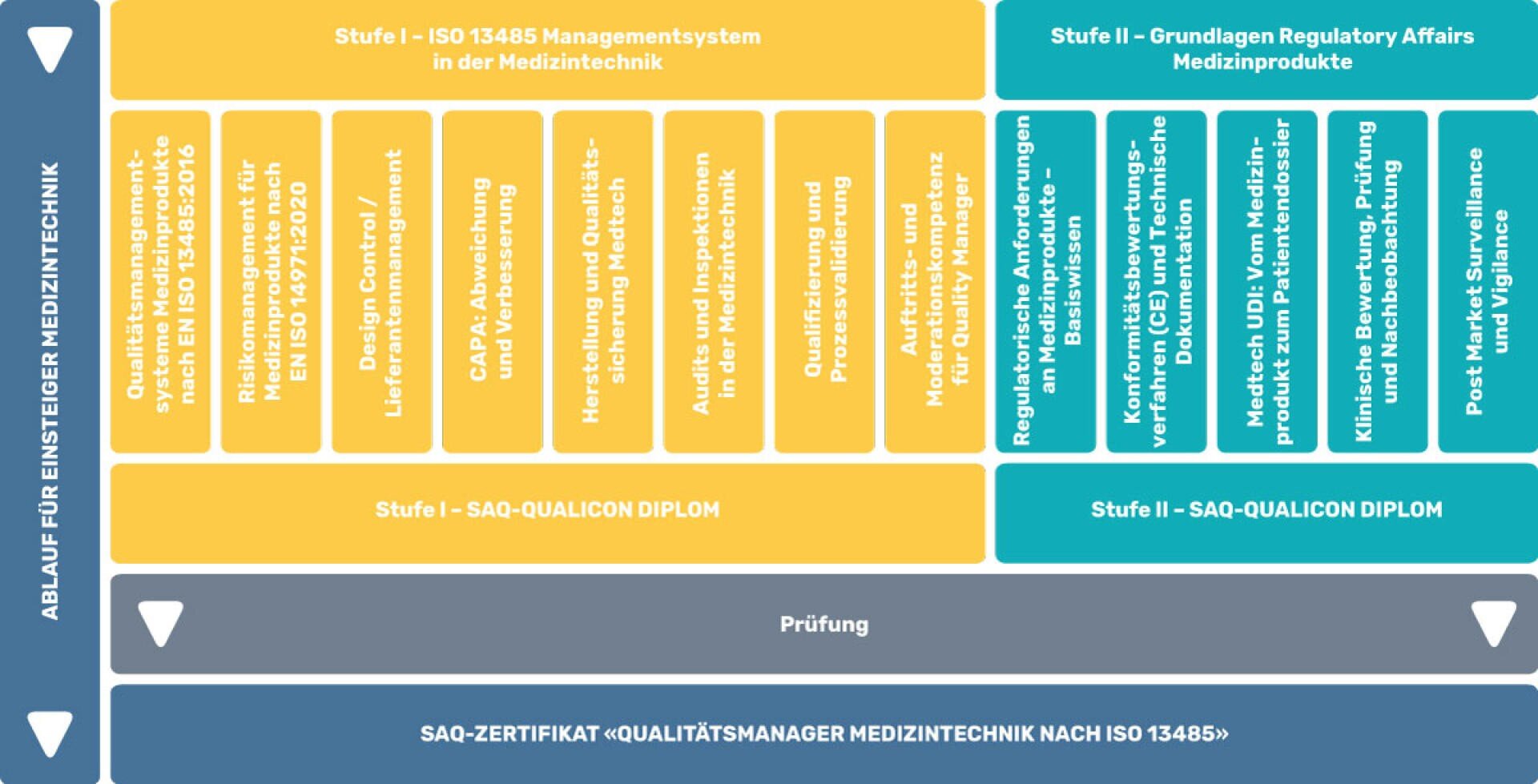
Stufe I - «ISO 13485 Managementsystem in der Medizintechnik»
Die Weiterbildung vermittelt die spezifischen Anforderungen an ein Qualitätsmanagementsystem gemäss ISO 13485:2016. Die Teilnehmenden können die Vorgaben auf die eigenen Bedürfnisse übertragen und ein entsprechendes Managementsystem optimieren.
- Qualitätsmanagementsysteme Medizinprodukte nach EN ISO 13485:2016
- Risikomanagement für Medizinprodukte nach EN ISO 14971:2020
- Design Control / Lieferantenmanagement
- CAPA: Abweichung und Verbesserung
- Herstellung und Qualitätssicherung Medtech
- Audits und Inspektionen in der Medizintechnik
- Qualifizierung und Prozessvalidierung
- Auftritts- und Moderationskompetenz für Quality Manager
Stufe II - «Grundlagen Regulatory Affairs Medizintechnik»
Die Weiterbildung vermittelt die regulatorischen Anforderungen (inkl. MDR/IVDR) über den vollständigen Lebenszyklus eines Medizinprodukts – von der Produktidee bis zum phase-out -, um diese zweckmässig im eigenen Berufsumfeld anzuwenden.
- Regulatorische Anforderungen an Medizinprodukte – Basiswissen
- Konformitätsbewertungsverfahren (CE) und Technische Dokumentation
- Medtech UDI: Vom Medizinprodukt zum Patientendossier
- Klinische Bewertung, Prüfung und Nachbeobachtung
- Post Market Surveillance und Vigilance
Weitere Informationen findest Du auf unserer Homepage.